鉄欠乏性貧血:軽症でも(どのくらいで)鉄を補充すべきか?
日本には鉄欠乏性貧血の乳児におけるガイドラインはない.
【臨床症状・検査所見】
症状:軽度~中等度貧血までは無症状が多い、細胞分裂が早い皮膚・粘膜症状が多い
心臓肥大、Restless leg症候群、舌乳頭萎縮、舌・口角炎、青色強膜、匙状爪、Pica、Pagophagia、難聴、精神運動発達障害
【診断と検査所見】
・貧血の定義:下図
ヘモグロビン濃度(g/dl)に基づいた貧血(Lancet 2006 387 10021 907-916より)
|
|
軽度 |
中等度 |
高度 |
|
6ヶ月〜4歳 |
11未満 |
10未満 |
7未満 |
|
5歳〜11歳 |
11.5未満 |
11未満 |
8未満 |
|
12歳〜14歳 |
12未満 |
11未満 |
8未満 |
・鉄欠乏症の定義:5歳未満 フェリチン<12μg/dl、5歳以上 フェリチン<15μg/dl
・鉄欠乏性貧血の定義:貧血+鉄欠乏症 (+他に原因がない)
CQ 軽症の鉄欠乏性貧血に鉄補充を行うべきか?
・学童期、青年期
貧血の有無に関わらず鉄欠乏症は認知機能障害を起こしうる。
Pediatrics. 2001;107(6):1381 より
・新生児/乳児/幼児
貧血の有無に関わらず鉄欠乏症は、精神発達障害を起こしうる。
そのため米国小児科学会では、発達への影響を予防するため生後4カ月からの鉄補充を推奨している。
生後6カ月を越えると母乳中の鉄のみでは必要量を満たさず鉄欠乏症になりやすい。しかし、日本では離乳期初期から十分な鉄を摂れる市販の離乳食がない。
日本では、乳児における鉄欠乏性貧血のまとまった報告が少なく、乳児期の鉄欠乏性貧血が無症状で一過性と考えられているため小児科医に関心をもたれていないことが問題である。鉄欠乏症では、鉄補充を推奨する。
小児科臨床. 2014;67(12):121-6 より
|
Take home message 貧血の有無に関わらず、鉄欠乏症は鉄補充を行う |
銅欠乏症、好中球減少
銅欠乏症による血球減少
2017年6月1日血液内科勉強会 A3用紙1枚で簡潔にまとめ
参考文献:Up to date 2017時点、血液内科第72巻第6号 820-824
Causes of neutropenia(Blood 2014;124:1251)

銅欠乏症は、二次性好中球減少症の原因である
【体内の銅代謝】
体内の全銅含有量は50-120㎎(新生児期~乳児は約12㎎)存在する
代謝経路:胃、十二指腸、空腸から銅トランスポーター(ATP7A)より吸収される
肝臓から体の各臓器には、セルロプラスミン(銅輸送蛋白)により運ばれる
*母乳は比較的少量の銅を含む。初期母乳は0.7mg/lの銅が含まれる。これは0.2mg/lに急速に低下し、WHO推奨銅摂取量よりも少なくなる。この時期の銅摂取量不足は、肝臓の貯蔵銅で補う。
【臨床的特徴・検査所見】
診断は、臨床的特徴と検査所見を総合的に判断する
症状:血球減少(図1)、神経障害(亜急性連合性脊髄変性症(VitB12欠乏)に類似)、認知障害、発達障害、骨粗鬆症、頭髪異常(少ない毛、縮れ毛)、筋力低下、難治性痙攣、発達障害
検査所見:血清銅の低下(30μg/dl以下)、血清セルロプラスミン低下(15㎎/dl以下)
*骨髄検査 骨髄異形成症候群と類似(小空胞を持つ赤芽球系細胞や赤芽球系の過形成、環状赤芽球、小空胞を持つ骨髄系細胞)
【銅欠乏症の原因】図2
先天性:Menkes病(メンケスP型ATPアーゼ:ATP7A異常、)
後天性:吸収不良症候群(炎症性腸疾患、Celiac病など)、胃十二指腸切除後/胃バイパス手術、慢性腹膜透析・血液透析患者、鉄・亜鉛過剰、Wilson病の治療過剰、不適切なミルク栄養未熟児、長期経管栄養、長期経静脈栄養

図1 Eur J Haematol 2008;80:523

図2 J Neurol 2010;257:869
厚生労働省が推奨する銅の1日推奨量
|
年齢 |
0-2歳 |
3-5歳 |
6-7歳 |
8-9歳 |
10-11歳 |
12-14歳 |
15歳以上 |
|
推奨量(㎎/日) |
0.3 |
0.4 |
0.5 |
0.6 |
0.7 |
0.8 |
0.8-1 |
【治療】先天性代謝異常症の課題と進歩 脳と発達2012;44:107-112 より
(成人)銅2mg/日の投与、ココアによる治療も報告あり
*Up to dateでは銅欠乏症の脊髄神経症ギアを有する場合毎日8㎎を1週間投与し、2週間目に6㎎、3週目に4㎎、その後は2㎎を投与する
(小児:Menkes病)脳内移行性がよいヒスチジン銅を使用。治療目標は、血清銅・セルロプラスミン値を正常に保つこと(投与2か月以内に血球異常は改善する)
ヒスチジン銅750μg/mlを0.5-1ml/回を2-4回/週の間隔で皮下注射する。治療開始が生後2か月以前だと神経障害が予防できる
アナフィラキシーショックにおけるアドレナリンの作用機序
結論から先にいう
肥満細胞/好塩基球からのメディエーター放出の抑制 が主
⇒血管透過性亢進を防ぐ根本的な治療
その他に
①血管収縮作用 ⇒血圧↑
②強心作用
③気管支拡張作用
急性細気管支炎での吸入は生理食塩水と高調性食塩水どちらが有益か?
JAMA Pediatrics 2017June 5
【背景】
急性細気管支炎における高張食塩水吸入の有効性について、エビデンスは一致していない。初発の急性ウイルス性細気管支炎乳児(6週から12ヶ月)に、3%高張食塩水または0.9%生理食塩水による20分×2回の吸入療法を割り付ける二重盲検RCTを行った(n=777)。
【結論】
24時間以内の入院は、高張食塩水群48.1%・生食群52.2%で有意差はなかった(調整リスク差 -3.2%)。Respiratory Distress Assessment Instrumentスコアの改善は、高張食塩水群で大きく(平均 -3.1 vs. -2.4)、Respiratory Assessment Change Scoreについても同様であった。中等度の有害事象(咳の悪化など)は、高張食塩水群で多く(8.9% vs. 3.9%)、重篤有害事象はなかった。
【評価】
最大規模のRCTで高張食塩水の利益は否定された。急性細気管支炎で吸入療法を行う場合には生理食塩水を用いるべきである。
百日咳の診断と治療、免疫グロブリン製剤
『Up to date, 乳幼児の百日咳の治療と予防』
・幼児は、重症合併症(無呼吸、肺炎、呼吸不全、痙攣、脳症)を発症し得る。
・咳発作のトリガー(運動、寒冷温、鼻汁や喀痰の吸入)は避ける。
・系統的レビューで、気管支拡張薬、コルチコステロイド、抗ヒスタミン薬、鎮咳薬の対症療法が百日咳患者に有益であることは証明されていない。(臨床医は経験的にβ2刺激薬吸入を行うが、百日咳患者のβ刺激薬投与によるリスク上昇は報告されていない)

*5日未満は推奨されていない。日本では百日咳にAZMは保険適応がない。
AZM:10㎎/㎏ 3日間と比較して効果に差がないとする文献もある(下記)
Eur J Clin Microbiol Infect Dis 1999 Apr; 18(4):296-298
幼児にAZM:3日投与(10㎎/㎏/日 連日)、AZM:5日投与(初日10㎎/㎏/日、2日以降5㎎/㎏/日 4日間)の効果を比較した。
17人のAZM:3日投与群、20人のAZM:5日投与群のうち、35例中33例(94.3%)の患者が治療開始7日後にBordetella pertussis培養は陰性だった。14日後に評価可能な34人の全患者が培養陰性であった。
マクロライド系抗菌剤と肥厚性幽門狭窄症
・アジスロマイシンとエリスロマイシンは、特に2週間未満の乳児で乳児肥厚性幽門狭窄(IHPS)のリスク増加と関連している〔Pediatrics. 2015 Mar;135(3):483-8〕
⇒結果研究期間中の1074236人のうち、合計2466人がIHPSを発症した。生後14日目のアジスロマイシン曝露は、IHPSのリスク増加を示した(調整オッズ比8.26)。15日から42日の暴露も増加(調整オッズ比2.98)した。エリスロマイシンは生後14日以内の暴露で増加(調整オッズ比13.3)、および15〜42日も増加(調整オッズ比4.10)した。生後43〜90日は、いずれのマクロライドとも関連がなかった。IHPSとAZM,EMの関連は生後2週間に最も強いが、2〜6週齢児でも低いが関連は持続する。
・クラリスロマイシンのIHPSのリスクは知られていない〔Drug Saf 2002; 25:929]
・IHPSは、新生児にマクロライド治療を行い1ヶ月以内に嘔吐する場合に注意が必要である。
・抗菌療法
症状発症の7日以内に投与されると、症状の持続時間を短縮し、接触者への感染を減少させる。
補足;
診断基準

診断フローチャート

抗菌療法
周囲への感染性減弱、有症時期を短縮することが目的
CAMとAZMは、EMと比較して吸収、胃酸抵抗性、組織移行性が良好で半減期が長く、下痢などの消化器症状が少ない。
AZMは百日咳の保険適応はない。保険適用外だが、10㎎/㎏/日分1内服 5日間を推奨
免疫グロブリン製剤について
免疫グロブリン製剤(Up to dateに記載なし)
抗百日咳毒素抗体(抗PT抗体)による毒素中和目的に投与されるが、本邦では重症症状の軽減に有効であった報告が散見されるものの海外では否定的な論文が多い。
Novel therapies for the treatment of pertussis disease.〔Pathog Dis 2015 Nov; 73(8): ftv074〕より
1999年にBrussらが、26人の百日咳に感染した乳児において、免疫グロブリン製剤の複数静注を実施。P-IGIVの投与は、血清抗-PT抗体価の上昇、リンパ球増加の低下および発作性咳の減少をもたらした〔Pediatr Infect Dis J. 1999; 18:505-11。〕。ただし、残念なことに、2007年のハルパリンらの多施設試験は発作性咳の改善に何ら利点見つからなかった〔Pediaric infect Dis J 2007 Jan;26(1):79-81.〕。違いが生じたDissucusionとして前者と後者では、対象の年齢平均が前者:9.7週間、後者2.3か月である点に留意が必要である。
百日咳患者に対するガンマ・ベニンの使用経験 小児科臨床 32(1): 175-179, 1979.より
百日咳患児12例にγグロブリン:100mg/kgを2~7 日間隔で2~3回投与した。第2病週以内に使用すると、痙咳発作の回数は半減し、白血球も減少した。有効率は71%であった。
重症乳児百日咳における経静脈的ガンマグロブリン投与の有用性の検討
日本小児呼吸器疾患学会雑誌 19(suppl): 90-90, 2008.より
【緒言】重症乳児百日咳に対する経静脈的ガンマグロブリン投与(IVIG)の効果について検討を行った。
【方法】過去20年間に当院に入院した乳児百日咳症例について後方視的検討を行った。呼吸補助療法と呼吸循環監視を要した症例を重症例と定義し、IVIGの有無により重症例を2群に分け検討を行った。
【結果】乳児百日咳51例中19例が重症例と判断された。IVIGを受けた5症例は全て重症例であり、ガンマグロブリン200-400mg/kg/日3日間投与で行われた。重症例はIVIG施行群5例、非施行群 14例に分かれ、背景因子の比較では2群問に有意差はなかった。また2群間で人工呼吸管理を要した症例の割合に差はなく、IVIG施行群では3例が人工呼吸管理開始後にIVIGを開始された。IVIG後に得られた効果は症例により異なり、無呼吸の減少,気管支攣縮の減少,酸 素化の改善,低換気の改善が認められた。IVIG 施行群は非施行群に比して入院期間が有意に短かった。
【考察】百日咳に対するIVIG投与については、従来痙咳の軽減が主な評価項目とされてきた。しかし乳児では特徴的な症状を呈する頻度が低く、高頻度に呼吸補助を要するため、別の評価基準が求められる。本検討では重症乳児百日咳に対するIVIGが入院治療期間の短縮をもたらす可能性が示された。
出血性膀胱炎(定義、原因、症状、治療、予後)
小児科診療 2000年 第63巻 4号 570-574より大部分抜粋
【概念、病因】
肉眼的血尿と膀胱刺激症状を主徴とする膀胱炎を出血性膀胱炎と称し、時に発熱を伴う。
毒素、薬物、放射線、ウイルス/細菌による膀胱移行上皮および血管への損傷が出血性膀胱炎につながる1)。
ウイルス性出血性膀胱炎は、健常小児の頻度は少なく、移植後の免疫不全状態の小児に多い。また、大腸菌による出血性膀胱炎もあり、細菌感染にも注意をする必要がある。
膀胱内凝血塊による膀胱タンポナーデ・尿閉・腎後性腎不全に注意が必要である。膀胱タンポナーデの状態は、強い腹痛や下腹部の膨隆を認める2)。
尿沈渣では非細菌性の膿尿をしばしば認める。血小板数、凝固因子、腎機能測定、尿微生物培養、膀胱傷害の評価のため腹部超音波検査は、病態把握や鑑別有用である。
出血性膀胱炎の原因3)

出血性膀胱炎の原因薬剤2)

ウイルス性:
6-15歳に好発し季節的には3-10月に多く、1週間前後で軽快する予後良好な疾患で、確定診断は尿中からのウイルス分離・同定やペア血清での抗体上昇によってなされる。PCR法やPCR-RFLP法による同定検査が高感度で迅速診断が可能である。
多くはアデノウイルスが原因で、アデノウイルス出血性膀胱炎の起因血清は7型、11型、21型、34型、35型、37型が報告されている。このうち11型の頻度が最も高く、ついで21型が多い。その他、サイトメガロウイルス、ポリオーマウイルス、EBウイルス、単純ヘルペスウイルス、水痘帯状疱疹ウイルス、BKウイルスなどが病因となりうる。
報告された症例では、末梢白血球の上昇はなくCRP陰性、赤沈の正常~中等度亢進、尿蛋白2+まで認めた。いづれも膿尿を認めた。
薬剤性:
アルキル化剤(シクロホスファミド、イホスファミド、ブスルファン)、ペニシリン系抗菌剤、抗アレルギー剤(トラニラスト)、漢方薬(柴苓湯、小柴胡湯)の頻度が多い。
骨髄移植・放射線関連:
頻度は2-16%と言われ、移植から2-100日ほど発症する症例が大部分である。移植片宿主反応や免疫不全状態が遷延することによる潜在ウイルスの再活性化が原因と考えられている。
骨髄移植時の全身放射線による直接的な膀胱損傷も起こるが、続発する免疫不全が発症により関与する。特に骨髄移植患者の出血性膀胱炎ではBKウイルスの関与が報告されている1)
BKウイルスは、初感染は小児期で無症状が多く、初感染後は腎臓に潜伏する。成人の90%がBKウイルス血清陽性である。出血性膀胱炎を起こした同種骨髄移植患者の尿からBKウイルスDNAが80.8%で検出され、うち20.8%はBKウイルス血症であった1)。
【重症度】Drollerの重症度分類1)

【鑑別診断】
悪性腫瘍との鑑別が困難な場合は、細胞診や膀胱鏡検査、病理組織検査を行う。
特発性腎出血・尿道炎(→三分杯尿でどの分画に血尿が認められるかで診断可能)、腎炎、Wilms腫瘍、膀胱粘膜癌、腎癌
【治療・予後】
健康小児に発症した出血性膀胱炎と、移植度免疫不全状態にある児の出血性膀胱炎の病態には大きな相違があり、必然的にその治療と予後は隔たりが生じる。
感染性(ウイルス、細菌性):
ウイルス性は予後良好、報告例では症状改善まで6~12日を要した。大腸菌によるものは、肉眼的血尿の消失に1~9日(平均2.2日)を要した。
薬剤性:
薬剤中止によって治癒するとされている。しかし、アルキル化剤の中止後に10年たっても出血性膀胱炎を繰り返した報告がある2)
骨髄移植を受けている小児患者:
移植関連死亡率は出血性膀胱炎なし患者:21%、出血性膀胱炎(重症度Ⅲ~Ⅳ)あり患者:71%と報告されている1)
【治療】
ウイルス性膀胱炎:
通常は十分な水分補給と利尿を促すのみで経過観察する。
出血が多い時:
トラネキサム酸2~3mg/kg/日またはカルバゾクロムスルホン酸10mg/kg/日の使用、膀胱刺激症状に対する鎮静目的で、塩酸クロミプラミン1~2mg/kg/日などを対症療法的に投与する場合もある。その他の保存的止血法として、プロスタグランジン(PG)製剤によ る膀胱内注入療法,フェノール,ホルマリン,ミョウバン,局所用トロンビンによる膀胱内注入療法がある。(ミョウバン,局所用トロンビンが麻酔の必要がなく安全に施行可能な方法である)。その他、外科的方法として、動脈塞栓術や手術療法がある。
抗癌化学療法時:
シクロホスファミド,イホスファミド大量点滴時の副作用予防には①膀胱持続灌流、②水分補給、③メスナ投与 がある2)。
【経過】
ほとんどの例は、出血性膀胱炎の軽快とともに腎機能も改善されてくる。しかし、一部には高度の腎機能低下を きたし、改善の傾向を示さない症例には腎生検による組織診断を行うとともに、ウイルス原因によっては抗ウイルス薬を投与しながら経過観察する。
メスナについて2)
メスナはシクロホスファミド,イホスファミドを投与される患者には有用な薬である。メスナは静脈から投与後、酸化され血清中で安定したジスルフィドになる。これは尿中でアクロレインと結合し不活性なチオエーテルになり排泄される。シクロボスファミドやイホスファミドの血中半減期は6-7時間であるがメスナの血中半減期は90分であるため、メスナが化学療法中に膀胱に存在するよう投与する必要がある。
高用量のシクロホスファミドやイホスファミドを投与された患者は少なくとも1日 2Lの飲水が励行され、寝る前まで飲水をし、夜間も一度は膀胱を空虚にするために排尿するべきである。ただし、膀胱刺激症状だけでシクロホスファミドの治療を中止する必要はない。
1) Pediatric hemorrhagic cystitis. J Pediatr Urol. 2009 Aug;5(4):254-64
2) 日本臨床 2012年 70巻 増刊号6 432-437
IgA血管炎の小児と成人の違い
IgA血管炎は、IgAを含む免疫複合体の沈着を伴う全身性の小血管炎で、血小板減少および血液凝固異常を伴わない紫斑性皮疹が出現する。IgAにはIgA1とIgA2の2つあり、その内IgA1のみが関与する。
皮膚症状はPalpable purpura、丘疹、紅斑、膨疹、血管浮腫であり、成人では血疱や潰瘍形成も多くみられる。〔日本皮膚科学会雑誌:127(3). 299-415.2017〕
小児では年間8~20.4人/10万人、成人では1.3人/10万人である。小児IgA血管炎(20歳未満)は、男女比:1.2-1.6であるが、成人の男女比は同等だった。腎疾患のは小児30-40%、成人45-85%で成人に多い。年齢は、2.5歳~88歳まで報告があり、平均年齢は小児:6.89±3.69歳、成人43.5歳±18.6歳だった〔J Korean Med Sci. 2014 Feb;29(2):198-203〕。
<15歳未満の年齢分布>〔Asia Pac Allergy. 2014 Jan;4(1):42–47〕
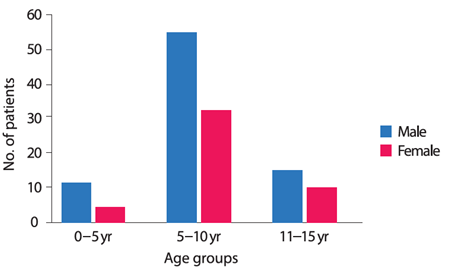
【原因】〔J Korean Med Sci. 2014 Feb;29(2):198-203〕
発症は、春と冬に多い。成人は、悪性腫瘍や薬剤によるIgA血管炎の頻度が小児より高い。

過去に報告された原因〔Pharma Medica.Vol.26 No.5 2008〕

【小児と成人例の比較】
<小児と成人の症状>〔Pediatr Neonatol. 2009 Aug;50(4):162-8〕

腹痛と発疹の間隔は1-21日までの範囲(中央値:8.3±5.52日)であった。
血尿の出現は小児で第1週間目33%、2週目67%、成人で2週以内34%、5週以内67%であった。
小児では腹痛が発疹に先行することが多い(腹痛が先:小児 24.6% 成人 4.55%, P<0.05)。
<IgA血管炎のの初発症状>〔Asia Pac Allergy. 2014 Jan;4(1):42–47〕

<小児と成人の検査結果>〔Pediatr Neonatol. 2009 Aug;50(4):162-8〕

白血球数は小児例で優位に高い。
補体低下、IgA上昇、抗核抗体陽性率は成人例で高いようにみえるが、有意差なし。
IgA血管炎の診断にIgA組織沈着を証明する必要があるか?
日本皮膚科学会雑誌:127(3)。299-415.2017より
IgA血管炎は、IgA抗体が関与する小型血管炎である。
血小板減少および血液凝固異常を伴わない紫斑性皮疹(100%)が出現する。
皮膚症状は下肢を中心に出現するが、時に体幹や上肢にも出現する。
Palpable purpura、丘疹、紅斑、膨疹、血管浮腫であり、成人では血疱や潰瘍形成も多くみられる。
IgA血管炎の診断にIgAの組織沈着を証明する必要があるか?

EULAR/Presによる小児血管炎分類基準によると、蛍光抗体直接法(direct immunofluorescence;DIF)でIgA沈着の証明を行わなくてもIgA血管炎の診断が可能である。これは、小児血管炎の多くがIgA血管炎であるため、他の小型血管炎の可能性がほとんどないからである。

一方、初発年齢が21歳以上の成人発症のIgA血管炎の診断には、皮膚あるいは腎のIgA沈着を証明することを推奨する(推奨度:B)
腎生検が全例に施行困難であることを考慮すると皮膚小血管壁のIgA沈着の証明の意義は高い。しかし皮膚DIFは擬陽性と偽陰性が多いことから、その結果判定は慎重になさなければならない。
<小児における全身血管炎の頻度>Proceedings of Singapore Healthcare 2012. Vo21.(4). 265-271

IgA血管炎、次いで川崎病が多い。MPA、Wegener’s granulomatosis、結節性多発動脈炎は少ない。
小児における市中C. difficile感染症
Risk Factors for Community-Associated Clostridium difficile Infection in Children
J Pediatr 2017;186:105-9
小児入院患者でCDIは増加し、死亡率の増加や入院期間の延長・入院費用の増加を招いている。近年では成人および小児において市中感染が増加してきている。現在では全CDI症例のうち1/3が市中CDI(Community-associated Clostridium difficile Infection:CA-CDI)である。CA-CDIの小児例ではPPIの使用と経腸栄養器具の使用が関連していると既報がある。
【目的】小児の市中クロストリジウム・ディフィシル感染症(CA-CDI)に関連する投薬および他の要因の特徴を示す。
【研究デザイン】米国の軍事保健システムデータベースの記録を用いて症例対照研究を行った。CA-CDI症例には、2001年から2013年までの外来患者のCDIを有する1歳〜18歳の子供が含まれた。過去12週間の薬剤曝露、最近の外来受診、1歳未満の兄弟姉妹への接触、CDIを有する家族との接触の有無を評価した。
方法:
1歳未満の小児は、頻繁に腸内にC difficileが常在化するため除外した。
以前入院中にCDIと診断した患者も除外した。12週間のうち、外来受診、1歳未満の兄弟姉妹の有無、CDIの診断を受けた家族に曝露したことを評価した。
【結果】対象群3993人とCA-CDIを有する1331人を比較した。
CA-CDI症例および対照の年齢中央値は7.0歳(3.3-13.4)であった。
症例は男性(50.3%)と女性(49.7%)で均等であった。
CA-CDIを有する1331人が複数の抗生剤に暴露されていた。うち795人(59.7%)は、CDI診断前12週間以内に抗生物質暴露があったが、40.3%には先行する抗生物質曝露はなかった。
CA-CDIの診断前12週間以内に抗生物質曝露を有した795人の小児のうち、319人(40.1%)は複数の抗生剤曝露を認めた。252人(31.6%)が2種類、68人(8.6%)が3種類以上の抗生剤暴露であった。
抗生物質処方後のCA-CDI発症までの中央値は33日(17-54日)であった。
図:小児市中CDIの傾向
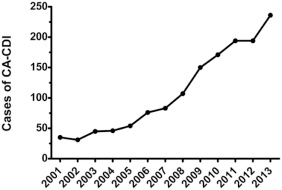
小児CA-CDI例は、12年間で47.9%の平均年間増加( P<.001)であった。
表:先行する抗生剤投与数によるC.difficileの感染率
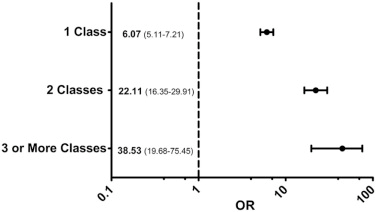
暴露された薬剤が多いほど、CA-CDIは増加する。
表:市中C. difficile発症にかかわる暴露因子の比較
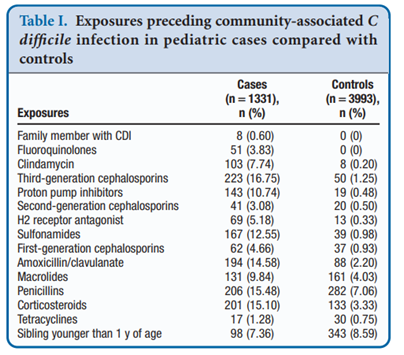
表:市中C. difficile発症にかかわる暴露因子の調整Odds比(Adjusted OR)

・クリンダマイシン、第3世代セファロスポリン、フルオロキノロン(CA-CDI群51例、対象群0でOdds算出はできなかった)は関連が高いと考えられる。
・注目すべきは、プロトンポンプ阻害剤(OR 8.17)曝露後のCA-CDIのオッズが、抗生物質クラスの曝露に匹敵している。
・最近の外来受診はCDI発症に関連し、受診のたびに35%ずつOddsが増加する(OR 1.35)
・CDIを有する家族との接触はCA-CDIと関連していた(CA-CDI群8症例、対象群0例)
・1歳未満の家族に対する接触はCA-CDIと関連しなかった(OR 0.83)
【結論】CA-CDIは、外来処方薬と、外来受診、CDI家族への接触 に関連している。
孫引き文献:Clostridium difficile infections in infants and children.
Pediatrics. 2013 Jan;131(1):196-200.
【C difficileのキャリア率について】
0-1か月: 約37%、Ⅰ-6か月: 約30%、 6-12か月:約14%、3歳以上はnon-hospitalized adultsと同等(0%~3%)。小児および成人の入院患者におけるキャリア率は、約20%である。
(他文献:Role of Clostridium difficile in childhood diarrhea.
Pediatr Infect Dis J. 1995 Jul;14(7):598-603.
0〜12歳の患者のうち、外来患者の2.9%、入院患者の4.6%、および対照の6.6%にCディフィシルが定着していた。)
CDIを発症した小児の関連因子は、抗菌薬治療、プロトンポンプ阻害剤の使用、反復浣腸、おむつの使用、長期経鼻胃管挿入、胃瘻および空腸瘻管、基礎腸疾患、胃腸管手術、腎不全、免疫不全があげられる。
C.ddifizileが原因となる臨床症状は、12〜24ヶ月児では稀である。新生児/乳児がClostridium種の毒素に結合して処理する細胞機構を欠いている可能性がある と推測されている。
CDIの検査
1歳未満の小児におけるCディフィシルの日常的な検査を避けることが賢明。下痢を伴う1歳から3歳の小児では、CDI検査が考慮されるが、下痢の他原因(特にウイルス性)の検査がまず推奨される。3歳以上の小児は、成人と同様に検査を行うことができる。
偽膜の内視鏡所見および直腸粘膜の発赤は、偽膜性大腸炎を示唆し、任意年齢でCDIを診断するのに十分である。
小児CDIの治療
CDI治療を受けた患者の30%までが、治療を中止した後に再発する。
メトロニダゾールは、2回目の再発(3回目のエピソード)や慢性的な治療(神経毒性の可能性があるため)の治療に使用すべきではなく、バンコマイシン内服が推奨される。
メトロニダゾールは、軽度から中等度の疾患を有する小児および青年の初期治療に選択される。重度患者および経口メトロニダゾールに応答しない患者に、経口バンコマイシンは初期治療として選択される。
経口メトロニダゾール(4回に分けて30mg/kg/日、経口、最大2g/日)
経口バンコマイシン(4回に分けて40mg/kg/日、最大2g/日)
症候性の患者には、手袋を使用し石鹸と水で手を洗う。塩素製品を使用して環境汚染を除去することが重要な管理策である。下痢が解消したら、管理策は解除できる。
抗不整脈の使い方(Ⅰ群薬の入門)
抗不整脈薬

誰も教えてくれなかった 循環器薬の選び方と使い分け(2017/3/30発行)より
Sicilian Gambit分類とVaughan Williams分類の両方を考えると理解しづらいため、まとめ。単純なVaughan Williams分類でまずは理解をすすめる。
Ⅰ群薬
使い分けのポイント:
【分類】
心筋細胞の活動電位の持続時間(QT時間)の作用で分類
- 活動電位の持続効果
- チャネルへの結合・解離速度
Naチャネルの主要な作用は活動電位を発生させること。活動電位のごく最初に作用する。
心筋の興奮時の作用:
Naチャネルがひらく→Naチャネルブロッカーが結合する→次の興奮から作用する
(最初の興奮で結合したなチャネルブロッカーが次の興奮まで残ることで、次の興奮の最初にチャネルをブロックできるので作用が発揮される)
|
|
代表薬 |
① 活動電位持続時間(QT間隔)に対する作用 |
②チャネルへの月結合・解離の速度 |
③親和性の高いチャネルの状態 |
|
Ⅰa群薬 |
キニジン プロカインアミド(アミサリン®) ジソピラミド(リスモダン®) ジベンゾリン(シベノール®) ピルメノール(ピメノール®) アジマリン(アスペノン®) |
延長 |
中等度 |
活性状態 |
|
Ⅰb群薬 |
リドカイン(キシロカイン®) メキシレチン(メキシチール®) |
短縮 |
早い |
不活性状態 |
|
Ⅰc群薬 |
フレカイニド(タンボコール®) プロパフェノン(プロノン®) ピルシカイニド(サンリズム®) |
不変 |
遅い |
活性状態 |
アプリンジンはⅠb群薬だが、性質がⅠa群薬に近いためⅠa群薬に分類
①⇒Ⅰa群薬はQTを延長させる、Ⅰb群薬は短縮、Ⅰc群薬は不変
②⇒結合・解離速度が速いⅠb群薬は、収縮時間が短く拡張期が長い心房筋では拡張時間の間にチャネルから外れてしまうので心房性不整脈には作用せず心室不整脈だけに使用する薬物と考えることができる。Ⅰc群薬は結合解離速度が遅いので、頻脈じゃない洞調時も比較的長い拡張期でもチャネルからかい離しないのでブロック作用を発揮するため、Baseの心電図でQRS時間の延長を示すことがある。
端的に言うと、Ⅰb⇒心室性不整脈だけ、ⅠaとⅠc⇒心房・心室不整脈の両方に使用可
③⇒専門的なので割愛
【QRS時間とQT時間】
QRS時間の延長は催不整脈作用に関連する⇒QRS時間が延長している場合はⅠc群薬の使用は避ける
QT時間が延長はTorsade de pointesを起こす⇒QT延長している場合はⅠa群薬の使用は避ける
【副作用】
Ⅰ群薬を選択するときは、どの薬が効きやすいか決めるのは至難。
そのため、副作用が起こりにくい薬を選ぶ ということが多い。
心臓副作用:3つが重要
・QT延長に伴うTorsade de pointes ⇒主に、Ⅰa群
・QRS延長に伴うCAST型不整薬 ⇒主に、Ⅰc群
・心機能抑制作用 ⇒Ⅰa群とⅠc群薬、理由は不明だが中でもジソピラミド・フレカイニドで心抑制作用が強い
非心臓作用:4つが重要
Ⅰa群の抗コリン作用
プロカインアミド以外。キニジン;下痢・悪心などの消化器症状、ジソピラミド;尿閉・口渇が多く前立腺肥大症、緑内障は禁忌。
ジソピラミド、シベンゾリンの低血糖
リドカインの神経作用
アプリンジンの肝障害・汎血球減少
◎実際の使い分け手順:
心房性不整脈では、Baseの心電図でQRS間隔が長い場合はⅠc群を避けて、Ⅰa群を選択する。QT間隔が長い場合Ⅰa群を避けてⅠc群を選択する。
心不全がある場合は可能ならⅠ群薬を避けて、どうしても使うならジソピラミド、フレカイニド以外を選択する。これらの制約がない場合は、Ⅰ群薬の副作用を考慮して前立腺肥大症や緑内障がある患者には、抗コリン作用がないプロカインアミドかⅠc群、糖尿病患者ではジソピラミド・シベンゾリン以外を選択する。
蛋白尿のアプローチ
蛋白尿へのアプローチ
小児の検尿マニュアル 日本小児腎臓学会編集より
Point:進行性疾患の発見、全身性(免疫/代謝/内分泌)・腫瘍・感染症・排尿異常の発見
病的蛋白尿:3歳以上では尿蛋白/尿Cre比が0.15g/gCr以上

ネフローゼ症候群:高度蛋白尿(夜間蓄尿で40㎎/時/㎡以上)または早朝尿で尿蛋白/Cre比:2g/gCr以上、かつ低Alb血症(Alb:2.5g/dl以下)
確認すべきRed flag sign(専門医へ早急に紹介:
-
問診: 体位性蛋白尿や運動、発熱などによる一過性蛋白尿を除外する
+α 血尿を伴う場合の問診鑑別

- 検査:生理的蛋白尿や低分子蛋白尿を除外する
最低限行う検査:
早朝第一尿、来院時随時尿 (尿定性は濃縮・希釈尿の影響を受ける。尿蛋白/尿Creは影響を受けない)、身長、体重、血圧、腹部超音波検査、尿沈渣、尿蛋白/尿Cre、総蛋白、Alb、Cre、BUN、補体、T-chol、尿中β2・α1 ミクログロブリン/尿Cre(尿PH6以下で分解され偽陰性化、10000μg/LはDent病疑い)、CRP、血沈
追加検査:
ASO、IgA、IgG、抗核抗体、シスタチンC、HBs抗原、HCV抗体
- 鑑別診断:

- 検尿異常のフォローと腎生検、専門医への紹介のタイミング

腎生検の推奨:
- ネフローゼ発症時に、①1歳未満、②持続血尿、③高血圧、④腎機能低下、⑤低補体血症、⑥腎外症状(発疹、紫斑など)
- ステロイド抵抗性を示すネフローゼ症候群
- カルシニューリン阻害薬の長期投与(投与開始2-3年後に腎生検で腎毒性を評価)
早朝第一尿の取り方

学校検尿のフローチャート:

新生児の頭蓋内出血
周産期医学 Vol.46 増刊号/ 2016 713-717より
病態:
側脳室周囲に存在する脳室上衣下胚層は、在胎25-26週で最大となり、以降は縮小傾向になる。
在胎32週以前の児では、脳室上衣下胚層に出血を起こした場合に脳室内出血となることが多い。
脳室上衣下胚層は、前脈絡叢動脈、内側線条体動脈、外側線状体動脈が支配し各々が内頸、前大脳、中大脳動脈の終枝で虚血やうっ血を含めた血流変化を受けやすい。
早産児の血管壁はコラーゲンや細胞成分に乏しく破綻しやすくIVHが発症しやすい。
在胎23-28週児の検討ではIVHなしは70.8%だった。
症状・診断:
特異的症状はなく、徐脈、無呼吸、大泉門膨隆、自発運動低下、筋緊張低下、痙攣などで気づく。
迅速性から診断は、頭部超音波検査が第一選択で重症はPapile分類(CT診断)、Volpe分類(頭部超音波検査)で行う。早産児のIVHは日齢3までに80%が起こるため定期的な画像検査を行う。
凝固能:ビタミンK欠乏に対するビタミンK2補充。凝固因子補充を目的としたFFP投与(10ml/㎏/回)
治療:
根本的な治療はない。出血後水頭症が進行する場合は腰椎穿刺、リザーバ留置、脳室腹腔内シャントを検討する。
予後:
原因不明の好酸球増加症のアプローチ
原因不明の好酸球増加症のアプローチ
参考文献:Up to date 『Approach to the patient with unexplained eosinophilia』
【病態生理】
好酸球は主に組織に分布する(血液の数百倍の分布)。
標的組織は、皮膚・肺・胃腸管が主であるが、深刻な臓器損傷は心臓・神経で起こる。
末梢好酸球数:1500/μlが臓器障害が起こりやすい臓器障害が起こりやすいと考えられているが、極端な場合を除き(2万/μl以上)、好酸球数は臓器障害のリスクを予測しない。
軽度:500-1500/μl、中等度:1000-5000/μl、高度:5000/μl以上
J Allergy Clin Immunol. 2010 Jul;126(1):39-44.
好酸球増加症の鑑別は、成人と同様である。
小児と成人の高カリウム血症の診断と治療管理①(総論)
【高カリウム血症の診断と治療管理 総論】
●Point:高K血症の基本事項を確認する
不足分は、小児の高カリウム血症の
高K血症の定義:原則(検査対象は)、血清カリウムが5.5mmol/lを超える
ただし新生児では基準値が高めとなる
K基準値:早産児 4-6.5mmol/l、新生児 3.7-5.9mmol/l、乳児 4.1-5.3mmol/l、1歳以上 3.5-5mmol/l
原因:
①腎排泄の減少
②過剰な摂取
③細胞内からの漏出
⇒ なので治療は、腎排泄を増加、摂取減少、細胞内へのカリウムシフト増加 する薬剤の投与となる
カリウムの排泄
主に腎臓で起こる。腎外排泄のメカニズムは、カリウムの細胞外シフトや胃腸からの漏出(毎日カリウム摂取量の約10%が胃腸管を介して取り除かれる)がある。
糸球体濾過率(GFR)が15ml /分/1.73m 2未満に低下するまで、腎カリウムホメオスタシスを維持可能である。
腎臓におけるカリウム調節機構
カリウムは糸球体で濾過され、Henleの近位尿細管およびループ脚でほぼ完全に再吸収される。排泄は主に皮質採集管で起こる。
ろ過されたカリウムの約20%は、Henleの太い上行脚に再吸収される。
腎外のカリウム調節機構
細胞内へのカリウムシフトを増加させる:インスリン、アシドーシス、アドレナリン、ノルアドレナリン、ドーパミン
カテコラミン機序⇒筋細胞上のβ2レセプターに結合するカテコラミンが細胞へのカリウムシフトを増加させる
インスリン機序⇒肝臓および筋細胞へのカリウム取り込みを増加させる
カリウムの摂取目安量
成人の値:男性 2,500 mg/日、女性 2,000 mg/日
小児は下記:
0~5 か月:400㎎/日、6~11 か月:700 mg/日、1-5歳は量的な詳細報告がなく目安量の設定が困難

カリウムの耐容上限量
腎機能が正常である限り、過剰摂取になるリスクは低い。したがって、耐容上限量は設定しない。ただし、腎機能が障害されている場合には摂取量に注意する。(厚生労働省食事摂取基準より)
一般的なカリウムが豊富な食品
カリウム(K) 1 mEq = 1 mmol ≒ 39 ㎎
|
食べ物 |
K含有量mmol |
食べ物 |
K含有量mmol |
|
バナナ(1個85g) |
8.6 |
オレンジジュース(200ml) |
7.9 |
|
ブルーベリー(100g) |
1.9 |
ミルク(200ml) |
7.7 |
|
マッシュルーム(75g) |
8.1 |
コカ・コーラ(200ml) |
0.1 |
|
ブロッコリー(75g) |
5.8 |
ポテトチップス(20g) |
5.1 |
|
納豆(75g) |
3.9 |
ミルクチョコ(20g) |
2.4 |
|
タマネギ(75g) |
1.5 |
ホワイトチョコ(20g) |
1.8 |
|
フライドポテト(150g) |
17.7 |
ワインガム(20g) |
1.8 |
|
玄米(150g) |
2.2 |
スパゲティ(150g) |
2.3 |
高カリウム血症の原因
カリウム摂取過剰:
①輸血
②K製剤
③ハーブ類など
腎機能や他の調節機構が正常なら、高カリウム血症を生じるために、極めて多量のカリウムが必要となる。腎機能障害(特にGFRが15未満)で起こりやすい
カリウム排泄障害:
①薬剤:ACE阻害剤/ARB/スピロノラクトン/エプレレノン/NASIDs/ヘパリン/シクロスポリン/タクトリムス/~ナゾール系の抗真菌薬/ST合剤/ペンタミジン
②急性/慢性腎機能不全(特にGFR<15はカリウム腎排泄の減少をもたらす)
③低アルドステロン症
④偽性低アルドステロン症
⑤先天性副腎過形成(約90%が21-ヒドロキシラーゼ欠損症)
⑥うっ血性心不全
⑦便秘症(カリウムの経腸排泄の減少)
細胞外への漏出:
①薬剤:β遮断薬/ジゴキシン/高浸透圧利尿剤/ST合材/サクシニルコリン/
②アシドーシス
③糖尿病(インスリン低下)
④高浸透圧(高血糖・マンニトール)
⑤組織壊死
⑥周期的四肢麻痺(骨格筋のNaチャネル変異)
高カリウム血症の診断
高カリウム血症の分類:
軽度(5.5-6.5mmol / l)、中等度(6.5-7.5mmol / l)重度(> 7.5mmol / l)
高カリウム血症は症状に関連することはまれ。
時に動悸、吐き気、筋肉痛、または感覚異常を訴える。
血清カリウム> 6.5mmol / lの患者では、心電図検査(ECG)の監視が必須。
検査は体系的で、常に心機能、腎臓および尿路の評価ならびに水分状態および神経学的評価を含むべきである。
参考文献:
・Up to date「Causes, Clinical manifestions, and evaluation of Hyperkalemia in Children」
・Pathogenesis, diagnosis and management of hyperkalemia. Pediatr Nephrol 2011 Mar; 26(3): 377–384.
・内科救急診療指針2016